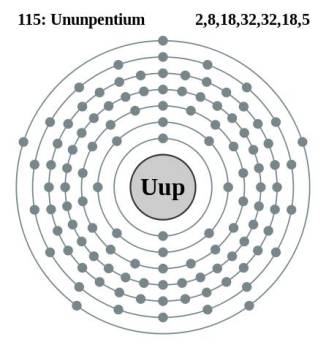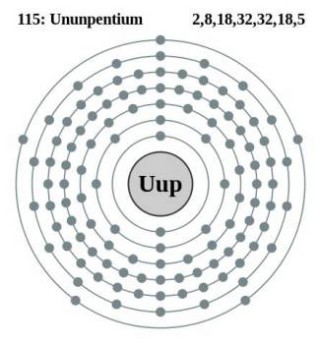
“Avvistato” per la prima volta nel 2003 da un gruppo di scienziati russi, presenta tutte le carte in regola per guadagnarsi un posto nella tavola periodica, tra il flerovio e il livermorio. Ma cerchiamo di capire perché l’ununpentio è così importante. Tra i vari parametri che caratterizzano gli elementi chimici vi è anche il numero atomico (Z), che indica quanti protoni sono presenti nel nucleo (più alto è il numero atomico, più l’elemento è “massivo”). Creare nuovi elementi chimici dopo l’uranio, l’elemento naturale con il maggior numero di protoni (ben 92) è stato possibile solo grazie agli esperimenti condotti nel corso degli anni dagli scienziati, bombardando elementi già esistenti con altre particelle. E’ in questo modo che, passando dal nettunio (Z 93) e dal plutonio (Z 94) si è giunti fino all’ununpentio con i suoi 115 protoni, ottenuto bombardando un sottile strato di americio (Z 95) con ioni di calcio (Z 20). Ma c’è una nota negativa nella scoperta: l’estrema instabilità dell’ununpentio che lo porta a decadere, ovvero a “trasformarsi” in un altro elemento (l’ununtrium con 113 protoni) in appena 173 millisecondi. La breve vita media degli elementi superpesanti è un vincolo a cui gli scienziati cercano di far fronte sviluppando sempre nuove teorie, tra le quali spicca quella del fisico Gleen Seaborg, nota come “Isola della Stabilità”. Essa prevede l’esistenza di elementi superpesanti particolarmente stabili con vite medie dell’ordine dei minuti o addirittura dei giorni.
Nell’attesa che la scienza faccia il suo corso, non resta che chiedersi “ma dovremmo comprare una tavola periodica nuova, o basterà ritagliare un quadratino e attaccarlo in quella vecchia!?”